В составе жидких радиоактивных отходов, образующихся при работе АЭС, самой вредной коррозионной примесью являются ионы Cl–, так как под их воздействием может развиться наиболее опасная локальная питтинговая («язвенная») коррозия – очень быстрое сквозное точечное разрушение нержавеющей стали. Развитие такого процесса не поддается прогнозированию, таким образом, при хранении ЖРО необходимо предусмотреть полное исключение вероятности коррозии такого вида.
Условия развития питтинговой коррозии
Известные способы борьбы с питтинговой коррозией состоят в разработке мероприятий, направленных на то, чтобы потенциал стенки оборудования имел меньшие значения, чем потенциал питтингообразования. Электрохимические методики наиболее подходят для определения сравнительной стойкости к питтингу различных марок сталей или определения потенциала питтингообразования в конкретной среде. Недостатком существующих в настоящее время методов определения пороговых концентраций ионов–активаторов (гальваностатической и потенциостатическая поляризации) является их зависимость от временного фактора, то есть отсутствует уверенность в том, что при большей длительности испытаний полностью исключена вероятность появления питтинга.
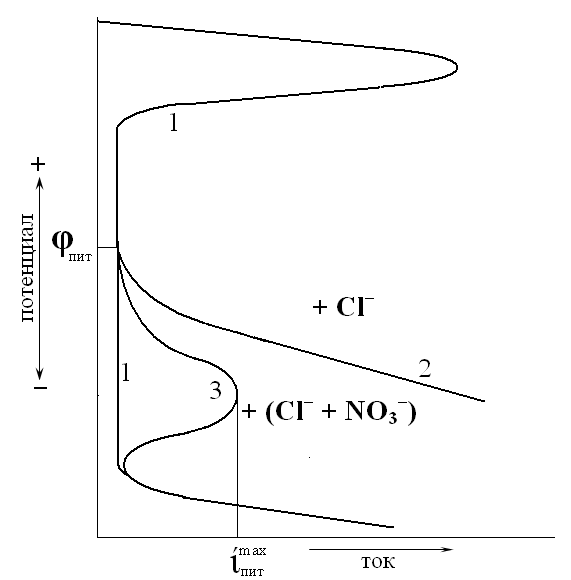
 Рис. 1. Схематическая анодная кривая для пассивирующейся нержавеющей стали (1) с добавкой ионов хлора (2) и в нитратно-хлоридной среде (3)
Рис. 1. Схематическая анодная кривая для пассивирующейся нержавеющей стали (1) с добавкой ионов хлора (2) и в нитратно-хлоридной среде (3)В ЖРО атомных станций, наряду с агрессивными ионами, присутствует и ион нитрата – компонент, потенциально способный подавлять развитие питтинга. Он препятствует или сильно затрудняет адсорбцию активаторов (Cl– ) на поверхности стали за счет вытеснения ионов Cl–, непосредственно участвующих в анодной реакции, протекающей внутри питтинга. В связи с этим очень важно определить такое соотношение ингибитора (нитрата) и активаторов в составе ЖРО, при котором полностью подавлена сама возможность развития питтинговой коррозии. При этом следует учитывать, что в присутствии нитратов развитие питтинга протекает по своим особым закономерностям, и при облагораживании потенциала скорость процесса меняется, проходя через максимум (рис.1 (3)).
Основное отличие данной методики состоит не в исследовании условий возникновения питтинга, а в определении состава среды, при которых подавляется уже функционирующий питтинг. Для этого первоначально искусственно создавалась интенсивная коррозия, а в дальнейшем относительное содержание агрессивного компонента в составе раствора снижалось вплоть до полного подавления питтинга. Основанием для методики послужило то обстоятельство, что в процессе питтинга постоянно происходит обмен раствора между внутренним объемом, в котором сосредоточено локальное растворение, и областью, не затронутой коррозией. При варьировании составом раствора в модельной проточной ячейке (снижении концентрации ионов Cl–, увеличении концентрации ионов NO3– или при совместном изменении обоих параметров) такой обмен в конечном итоге приведет к торможению анодной реакции в области развития питтинга.
 Рис. 2. а) Анодная потенциодинамическая кривая (1мВ/сек) на стали 12Х18Н10Т при 25°С в растворе 1М NaCl при рН=6; б) Изменение во времени плотности анодного тока на стали 12Х18Н10Т при постоянном потенциале 0,55 В в тех же условиях
Рис. 2. а) Анодная потенциодинамическая кривая (1мВ/сек) на стали 12Х18Н10Т при 25°С в растворе 1М NaCl при рН=6; б) Изменение во времени плотности анодного тока на стали 12Х18Н10Т при постоянном потенциале 0,55 В в тех же условияхВ нейтральной среде, при низком содержании нитрата или при полном его отсутствии (рис. 1 (2)), анодные реакции резко активизируются уже при незначительном смещении потенциала конструкционного материала (нержавеющей стали) в сторону увеличения относительно потенциала коррозии (рис. 2). Появление на анодной кривой характерного потенциала питтингообразования трактуется как результат того, что с ростом потенциала связи поверхности металла с ионами хлора становятся более прочными, чем с пассивирующим кислородом.
При фиксировании некоторого постоянного значения потенциала в области питтинговой коррозии плотность анодного тока некоторое время продолжает расти (рис. 2б) и в конечном итоге стабилизируется.
Изменение состава раствора при проведении лабораторных исследований проводили методом непрерывного разбавления, при котором рабочий объем ячейки оставался постоянным, но состав его непрерывно разбавлялся раствором с определенной концентрацией ингибитора или не содержащим хлорид. Такое лабораторное устройство аналогично реактору непрерывного разбавления, состав раствора внутри которого связан с объемом раствора, прошедшего через ячейку. Данный процесс можно описать уравнением
где V – объем системы;
∆V – объем электролита, прошедшего через систему;
Со – исходная концентрация ионов хлора в системе;
С – концентрация ионов хлора в определенный момент времени.
 Рис. 3. Относительная убыль концентрации хлорида (1) и прирост добавки ингибитора (2) в зависимости от кратности разбавления в реакторе непрерывного смешения
Рис. 3. Относительная убыль концентрации хлорида (1) и прирост добавки ингибитора (2) в зависимости от кратности разбавления в реакторе непрерывного смешенияТаким образом, регистрируя объем раствора, прошедшего через ячейку в определенный момент времени, можно для любого такого момента рассчитать концентрацию ионов хлора в электролите. В общем виде снижение концентрации компонентов при разбавлении исходной хлоридной среды раствором ингибитора характеризуется зависимостями, представленными на рисунке 3 (кривые 1 и 2).
«Антикоррозионный» состав ЖРО
Использование предложенной методики позволяет достаточно точно определить безопасное соотношение нитратов и хлоридов для полного предотвращения самой возможности появления питтинга. Если при постоянном значении потенциала регистрировать изменение во времени анодного тока на стали, интенсивно растворяющейся в режиме питтингования, можно проследить, как разбавление раствора приводит в конечном итоге к торможению анодной реакции в области развития питтинга. При достаточно медленном изменении состава раствора в объеме ячейки можно практически синхронно менять и состав среды внутри области питтинга. Торможение анодного процесса внутри питтинговой коррозии уверенно регистрируется по снижению тока. После подавления ингибитором (NaNO3) последних очагов локального растворения (рис. 4 (1)) прекращаются спорадические колебания тока во времени и он стабилизируется при некотором постоянном значении с небольшими плавными флуктуациями. При простом разбавлении хлорида раствором, не содержащим ингибитора (например, водой), не наблюдается затухания периодических колебаний (рис. 4 (2)).
 Рис. 4. Изменение во времени плотности анодного тока на стали 12Х18Н10Т в 1М NaCl при постоянном потенциале 0,55 В и непрерывном разбавлении раствором 2 М NaNO3 (1) и водой (2) при 25°С и рН=6
Рис. 4. Изменение во времени плотности анодного тока на стали 12Х18Н10Т в 1М NaCl при постоянном потенциале 0,55 В и непрерывном разбавлении раствором 2 М NaNO3 (1) и водой (2) при 25°С и рН=6Интенсивность процесса питтинга, искусственно созданного в чисто хлоридных средах, заметно снижается даже при незначительном разбавлении хлоридной среды раствором нитрата (рис. 5). Так, при соотношении NO3–/Cl–~ 0,3 происходит падение анодных токов на четыре порядка, тогда как дальнейшее 25-кратное увеличение этого отношения снижает токи растворения питтинга менее чем на порядок. Изменение анодного тока в зависимости от отношения NO3–/Cl– качественно идентично обратному ходу изотермы адсорбции. При конкурирующей адсорбции ионов снижение поверхностной концентрации ионов Cl–, регистрируемое по уменьшению анодного тока, обратно пропорционально росту степени заполнения поверхности ионами NO3–. Практическая стабилизация анодных токов при отношении NO3–/Cl–>0,3 соответствует переходу к предельному заполнению поверхности ионами нитрата, что полностью подавляет коррозионные процессы.
 Рис. 5. Зависимость плотности анодного тока на стали 12Х18Н10Т при потенциале 0,55 В от отношения NO3–/Cl– при разбавлении 1М раствора NaCl раствором 2 М NaNO3 при 25°С и значении рН=6
Рис. 5. Зависимость плотности анодного тока на стали 12Х18Н10Т при потенциале 0,55 В от отношения NO3–/Cl– при разбавлении 1М раствора NaCl раствором 2 М NaNO3 при 25°С и значении рН=6Данные по безопасному соотношению нитрата и хлорида, то есть по предельному заполнению поверхности ионами NO3– в зависимости от концентрации хлоридов, в обобщенном виде представлены на рисунке 6. Из их анализа следует, что концентрация нитрата, необходимая для полного подавления локальной коррозии на стали 12Х18Н10Т, увеличивается с ростом содержания хлорида в исходном растворе. Однако, другой параметр, так же характеризующий условия подавления питтига, – защитное отношение NO3–/Cl– – резко снижается по мере роста концентрации хлорида. Последнее, по-видимому, обусловлено тем обстоятельством, что полное вытеснение хлорида с поверхности связано с предельным ее заполнением ионами NO3–, которое мало зависит от концентрации хлорида. Количество нитрата в растворе, обеспечивающее полное вытеснение с поверхности ионов Cl– при минимальной исследованной их концентрации (0,07 М) составляет ~ 0,9 М, тогда как при последующем 300-кратном росте концентрации хлорида для полной защиты стали требуется увеличить содержание ионов NO3– на ~ 2,0 М, то есть менее чем в три раза.
 Рис. 6. Зависимость защитного отношения NO3–/Cl– для стали 12Х18Н10Т от содержания ионов хлора в растворе при 25°С и значениях рН=6 (1) и рН=12 (2)
Рис. 6. Зависимость защитного отношения NO3–/Cl– для стали 12Х18Н10Т от содержания ионов хлора в растворе при 25°С и значениях рН=6 (1) и рН=12 (2)В предложенной методике определения защитных соотношений ингибитора (NO3–) и активатора (Cl–) заложено некоторое превышение защитного соотношения, которое обусловлено рядом методических ужесточений условий ускоренных испытаний. Так, при проведении ускоренных испытаний материалу искусственно навязывается потенциал максимальной скорости развития питтинга, что дает возможность определить гарантированные условия для его подавления.
Проведенные исследования позволили построить номограмму, с помощью которой можно определить наличие или отсутствие питтинговой коррозии в емкостях-хранилищах ЖРО. Она оперирует данными об относительном содержании нитрат-ионов, хлорид-ионов и рН.
На основе данной методики и содержании нитрат-ионов в реальных ЖРО было выдвинуто предположение об отсутствии питинговой коррозии нержавеющей стали емкостей для хранения ЖРО на Нововоронежской и Курской АЭС. Результаты проведенных коррозионных испытаний с установкой образцов-«свидетелей» подтвердили правильность этого предположения.
Авторы:
Ю.И. Кузнецов, д.х.н., В.П. Разыграев, к.х.н., М.В. Лебедева, А.И. Щербаков, д.х.н., (Институт физической химии и электрохимии РАН)
Ю.П. Корчагин, к.т.н., Е.К. Арефьев (ОАО «ВНИИАЭС»)