Испанские исследователи разработали способ отслеживания особенностей распределения в биологических системах кластерных комплексов бора, применяющихся в качестве переносчика бора для такого перспективного направления онкологических заболеваний, как бор-нейтрон-захватная терапия [boron neutron capture therapy (BNCT)].
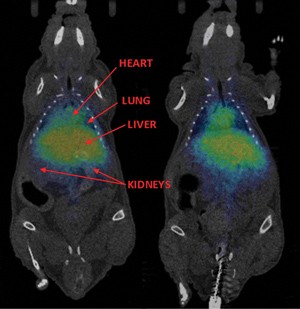
Распределение производных COSAN в организме крысы в режиме реального времени. (Рисунок из Chem. Commun., 2014, DOI: 10.1039/c4cc05058d)
Лекарственные препараты, основой которых является кластерный комплекс бора COSAN (кобальтабисдикарболлид – cobaltabisdicarbollide) использует то, что в клетках опухоли наблюдается сверхэкспрессия рецепторов мембраны , что позволяет доставлять через мембрану терапевтические дозы нуклида 10B. Несмотря на то, что 10B стабилен, если облучить клетку пучком нейтронов, ядро 10B захватывает нейтрон и затем распадается, высвобождая обладающую высокой энергией α-частицу, разрушая клетку.
Несмотря на перспективность, главной помехой в разработке такого типа терапии являлся недостаток методик, позволяющих эффективно определить эффективность аккумулирования бора in vivo, что, очевидно, затрудняет скрининг эффективности кандидатов в лекарства.
Клара Виньяс (Clara Viñas) из Института Материаловедения Барселоны с соавторами разработала стратегию ковалентного связывания производного COSAN либо с позитронным эмиттером 124I или эмиттером гамма-частиц 125I, таким образом, за распределением в организме лекарственного препарата можно следить как с помощью позитронно-эмиссионной томографии [positron emission tomography–computed tomograph (PET-CT, так и с помощью подсчета γ-квантов. Исследователи использовали катализируемую палладием реакцию обмена производного COSAN, чтобы ввести в препарат один из радионуклидов йода до проведения исследований на мышах in vivo, позволяющих количественно определить попадание препарата в клетки. Исследование показало, что результаты измерения обоими способами (за счет подсчета позитронов и за счет подсчета γ-квантов) хорошо согласуются между собой, что позволяет Виньяс и ее коллегам надеяться на то, что новый способ введения метки в производные COSAN.
Введение в соединения радиоактивных изотопов йода позволяет отслеживать соединения в организме in vivo. (Рисунок из Chem. Commun., 2014, DOI: 10.1039/c4cc05058d)
Виньяс поясняет, что хотя свойства кластеров бора во многом похожи на свойства органических соединений, они представляют собой неорганические вещества и, следовательно не могут быть разрушены в результате воздействия ферментов клетки, что делает их перспективными веществами для применения в медицине.