Химиотерапия – один из основных наиболее эффективных методов лечения онкологических заболеваний, однако его применение сопряжено с рядом сложностей. Лекарства не всегда бьют "точно в цель" по раковым клеткам и способны вызывать повреждения здоровых тканей. При этом некоторые клетки опухоли иногда могут оказаться устойчивыми к стандартной химиотерапии.
Ученые работают над адресными способами доставки лекарств в опухоль. В частности, для этого применяют микрокапсулы на основе наночастиц.
Учёные Курчатовского комплекса кристаллографии и фотоники НИЦ "Курчатовский институт" и Института биоорганической химии им. академиков М.М. Шемякина и Ю.А. Овчинникова РАН разработали новый вариант биоразлагаемых наноразмерных полимерных капсул. Они созданы методом послойной сборки полимеров на частицах-темплатах с последующей термоусадкой. Эта методика позволила уменьшить их размер и существенно повысить способность проникать в клетки (до 3,5 раз эффективнее, чем исходные образцы).
"Внутри капсул находится химиотерапевтический препарат доксорубицин, а на поверхности – специально модифицированный белок DR5-B. Достигнув поверхности раковых клеток, DR5-B связывается только с одним "сигнальным" рецептором – DR5, рецептором смерти, – рассказывает Дарья Трушина, старший научный сотрудник лаборатории биоорганических структур Курчатовского комплекса кристаллографии и фотоники. – В отличие от других вариантов этого белка, он не взаимодействует с иными рецепторами, которые могут блокировать сигнал и защитить опухоль. Поэтому DR5-B запускает гибель раковых клеток более эффективно, помогая обойти их устойчивость к лечению".
Таким образом, главная особенность новых нанокапсул – сочетание двух механизмов воздействия. Это направленная доставка препарата (что почти в 2 раза эффективнее, чем использование некапсулированной формы доксорубицина), и активация программируемой гибели опухолевых клеток.
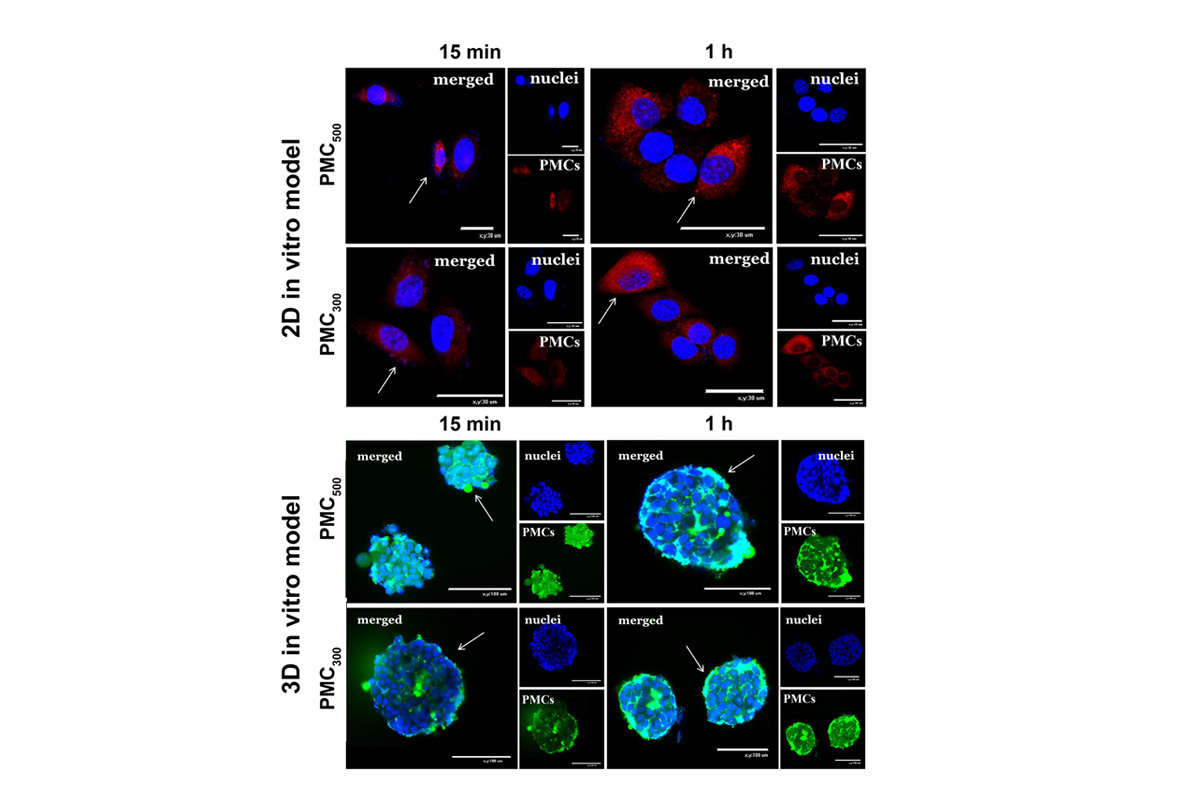
Обычно для тестирования лекарств в лабораторных условиях используют двумерные модели, где клетки выращивают в виде монослоя. Однако ученые также использовали трёхмерные сфероиды из опухолевых клеток, которые более точно имитируют структуру реальной опухоли при раке молочной железы.
Ключевой результат работы – обнаружение синергетического эффекта: даже в условиях трёхмерной клеточной модели комбинация доксорубицина и DR5-B позволяет эффективно уничтожать клетки опухоли, устойчивые как к химиотерапии, так и к действию DR5-B-подобных молекул. При этом здоровые клетки не повреждаются.
Новая методика может стать важным шагом в разработке персонализированных методов химиотерапии рака молочной железы.